Een verbinding kan kristalliseren met meer dan één structuur. Het is hetzelfde molecuul, maar het stapelt zich op in de ruimte in verschillende vormen, waardoor er verschillende kristallijne structuren ontstaan. Ze worden polymorfen genoemd, en het fenomeen staat bekend als polymorfisme. Het is van vitaal belang.
Elk van deze polymorfen heeft zijn eigen diffractiepatroon: ze hebben elk een andere identiteitskaart. En wat nog belangrijker is, hun fysische en chemische eigenschappen zijn verschillend. We hebben het over grafiet en diamant, aragoniet en calciet, maar ook over chocolade en medicijnen.
Eenzelfde molecuul kan in verschillende vormen kristalliseren. Een eenvoudig voorbeeld zal u helpen om dit te begrijpen. Laten we een kristal maken waarvan de eenheidscellen munten zijn. We kunnen dat op twee verschillende manieren doen. Met andere woorden, met twee verschillende structuren:


Een vierkante structuur (rechts) en een zeshoekige structuur (links). De verschillende structuren waarin dezelfde chemische verbinding kan kristalliseren worden polymorfen genoemd. Ondanks het feit dat ze dezelfde samenstelling hebben - in dit geval munten - hebben ze verschillende eigenschappen. Met het blote oog kunnen we zien dat de zeshoekige structuur dichter is (de munten laten kleinere tussenruimtes achter) dan de vierkante structuur.
In de wereld van de echte kristallen is dit structurele verschil van groot belang. Zo kristalliseert koolstof in twee polymorfen die de hele wereld kent: de diamant, die een kubusvormige structuur heeft, en grafiet, een gelaagde zeshoekige structuur.
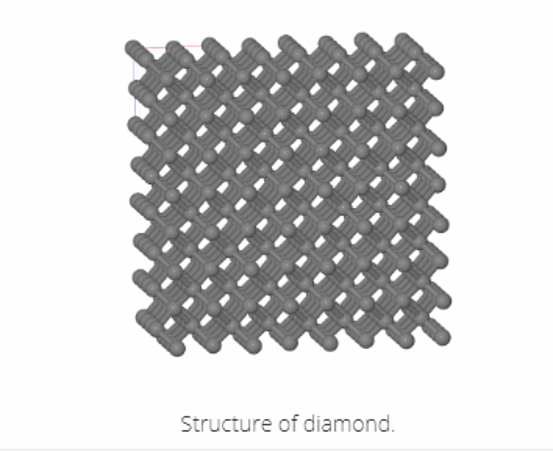
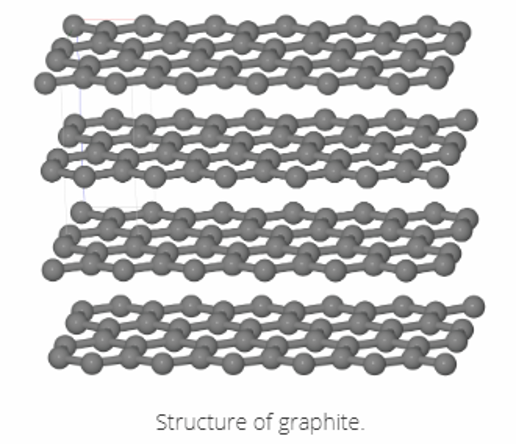
De eigenschappen van beide kristallen zijn zeer verschillend. Diamant heeft alle koolstofatomen die met elkaar verbonden zijn door covalente kristallen, waardoor het een extreem hard materiaal is, het hardste dat bekend is. Grafiet heeft echter een gelaagde structuur. De bindingen binnen de lagen zijn identiek aan die in de diamant. Toch zijn de bindingen tussen de koolstofatomen tussen de lagen veel zwakker. Dit maakt grafiet een zacht materiaal, want als we het drukken, bijvoorbeeld op papier, scheiden de lagen zich en blijven ze aan het papier kleven. Je weet natuurlijk dat dit de reden is waarom het lood van een potlood eigenlijk grafiet is.
Het hoofdbestanddeel van chocolade is cacaoboter, het vetzuur van cacao, gekristalliseerd. De moleculen van het cacaovetzuur kunnen kristalliseren tot zes verschillende structuren - zes polymorfen. Elke cacaovetzuurpolymorf heeft een verschillend smeltpunt:

Chocolade met polymorfen van I tot IV, met lagere smeltpunten, smelt heel gemakkelijk, waardoor het moeilijk is om ze uit de verpakking te halen en ze onze vingers bevlekken als we ze vasthouden. Chocolade gekristalliseerd uit polymorf VI heeft het aspect van dat witachtige kristalheldere poeder dat na verloop van tijd "bloeit" wanneer de chocolade wordt blootgesteld aan plotselinge temperatuurschommelingen - het herkristalliseert. Polymorf V, met een smeltpunt van 33,8, is degene die moet worden verkregen zodat de chocolade langzaam en aangenaam smelt in de mond.
Polymorfisme is van buitengewoon belang voor de farmaceutische industrie. In veel gevallen kristalliseert hetzelfde geneesmiddel met verschillende structuren, in verschillende polymorfen. Zo vormen bijvoorbeeld minstens 67% van de steroïden, 40% van de sulfonamiden en 63% van de barbituraten polymorfen.
Het molecuul, dat de actieve verbinding is, is hetzelfde in de verschillende polymorfen, en wanneer we een geneesmiddel nemen lost het op. Waarom is polymorfisme dan een probleem? Omdat, zoals u al weet, de eigenschappen van elke polymorf anders zijn. Stabiliteit, oplosbaarheid, oplossnelheid en biobeschikbaarheid zijn afhankelijk van de polymorf waarin het medicijn kristalliseert. Het beheersen van polymorfe kristallisatie is cruciaal voor elk farmaceutisch bedrijf.
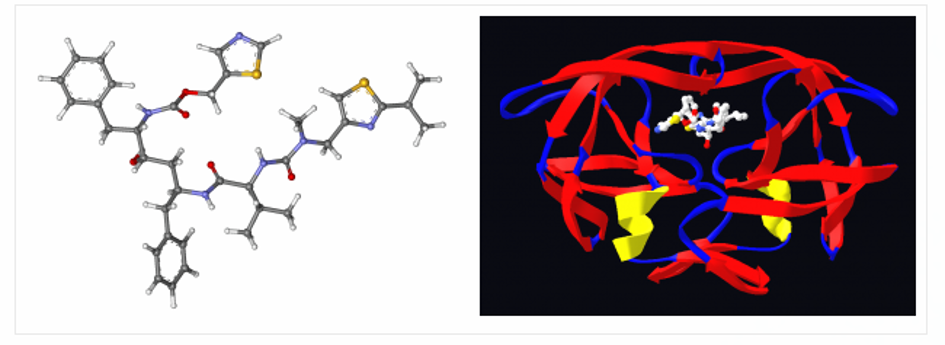
Een typisch voorbeeld van dit probleem is het geval van Norvir, een geneesmiddel (links) voor de behandeling van patiënten die besmet zijn met humaan immunodeficiëntie-virus type 1, dat werkt door het afremmen van de protease (rechts). Gekristalliseerd met een structuur die uniek werd geacht, slaagden sommige partijen na enkele jaren op de markt niet voor de oplosbaarheidstests. Men ontdekte dat het geneesmiddel tijdens het productieproces gekristalliseerd was met een stabielere structuur die langzamer oploste. Het product moest van de markt worden gehaald, nieuwe formules werden opnieuw geoctrooieerd, de kristallisatie werd bestudeerd en het hele productieproces werd opnieuw ontworpen, wat voor het bedrijf een verlies van miljoenen betekende.
Soms kunnen de gevolgen van een polymorfe overgang catastrofaal zijn, zoals in het geval van de polymorfe transformaties van ammoniumnitraat. Of ze kunnen economisch belangrijk zijn, zoals in het geval van calciumcarbonaat of gips. Want we weten nog steeds niet hoe we de polymorfe kristallisatie kunnen beheersen, of het nu gaat om ritonavir, ammoniumnitraat, calciumcarbonaat of vele andere verbindingen.

Het leven zelf weet dit echter met benijdenswaardige precisie te doen. Vogel-eierschalen zijn altijd gemaakt van calciet, een polymeer van calciumcarbonaat. Reptielen-eierschalen zijn altijd aragoniet, een ander polymeer van calciumcarbonaat. Bovendien weet het leven in schelpen van weekdieren zoals die van Haliotis (abalone) parelmoer met een aragonietstructuur te maken op slechts enkele micron van de buitenste lagen van calciet.
karaf, whiskykaraf, whiskey karaf, kristallen karaf, wijnkaraffen, wijnkaraf, kristal karaf, decanteer karaf, whiskey karaf kristal, kristal karaf, glazen karaf, karaf graveren, champagneglazen, whisky glazen, whiskey glazen.